Pfizer: koroonavaktsiin on 5 – 11-aastastele ohutu ja näitab tugevat antikehade reaktsiooni
(330)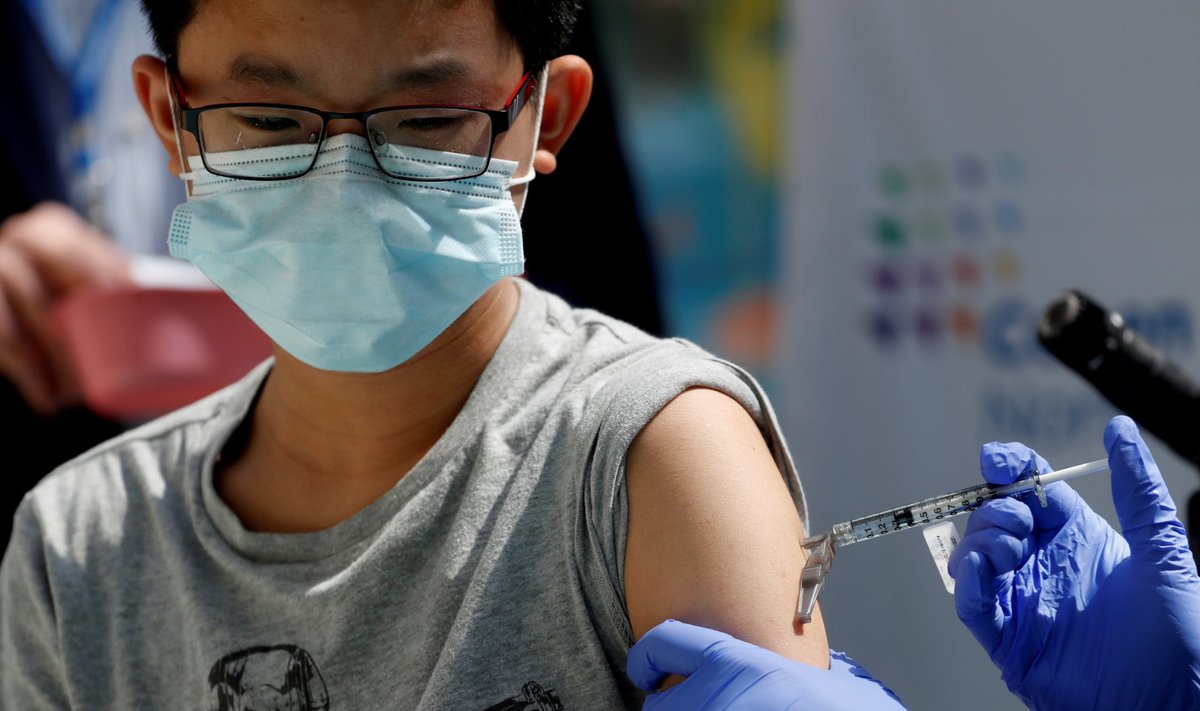
Ravimifirma Pfizer teatas täna, et teise ja kolmanda faasi katsetused näitasid, et Pfizeri koroonavaktsiin on ohutu ja tekitab tugeva antikehade reaktsiooni ka 5-11-aastastel lastel.
Tegemist on USA koroonavaktsiini jaoks esimeste selliste tulemustega selles vanusegrupis, kuigi andmeid ei ole veel retsenseeritud ega avaldatud. Pfizer teatas, et kavatseb esitada vaktsiini erakorralise kasutamise taotluse varsti USA toidu- ja ravimiadministratsioonile, vahendab CNN.
Katsetustel osales 2268 last vanuses 5–11 aastat ning kasutati kahe doosi režiimi. Kahe süsti vahele jäi 21 päeva. Üks doos oli 10-mikrogrammine. Alates 12. eluaastast kasutatakse 30-mikrogrammist doosi.
Katsetuses osalenute immuunreaktsioone mõõdeti, jälgides neutraliseerivat antikehade taset nende veres ja võrreldes seda 16–25-aastaste kontrollgrupiga, kes said kaks 30-mikrogrammist doosi. Pfizer teatas, et tase lastel oli võrreldav vanemate inimeste omaga, kes said suurema doosi, mis näitab tugevat immuunreaktsiooni sellel lastegrupil kuu pärast teist doosi.
Pfizeri teatel talusid lapsed koroonavaktsiini hästi ja kõrvalmõjud olid võrreldavad 16–25-aastaste vanusegrupi kõrvalmõjudega.
Pfizeri esindaja kinnitas, et ei olnud müokardiidi juhtumeid, mida on mRNA-vaktsiinidega seostatud.
Pfizeri teatel oodatakse veel selle aasta neljandas kvartalis katsetuste andmeid laste kohta alates vanusest kuus kuud.
„Alates juulist on COVID-19 pediaatriliste juhtumite arv USA-s kasvanud umbes 240 protsenti, mis rõhutab vaktsineerimise vajadust tervishoiu seisukohalt. Need katsetustulemused annavad tugeva aluse meie vaktsiinile loa taotlemiseks 5–11-aastastele lastele ja me kavatseme selle FDA-le ja teistele järelevalveorganitele kiiresti esitada,” ütles Pfizeri juht Albert Bourla.
